Katalizörler: Kimyasal ve Biyolojik Dünyanın Sessiz Kahramanları
1. Giriş: Katalizörlerin Tanımı ve Önemi
Katalizörler, kimyasal reaksiyonların hızını artıran, ancak reaksiyon sonunda tükenmeyen maddelerdir. Bu özellikleri, onları kimya dünyasında vazgeçilmez kılar. Katalizörlerin etkisi, yaşamın temel biyokimyasal süreçlerinden endüstriyel üretime kadar geniş bir yelpazeye yayılır.
1.1. Katalizörlerin Tarihsel Rolü
İnsanlık tarihindeki ilk katalitik süreçler, ateşin keşfiyle başlamıştır. Doğal olarak oluşan oksitler ve mineraller, metalleri işlemek ve seramikleri sertleştirmek için kullanılmıştır. Zamanla, bu süreçler bilimsel bir yaklaşımla ele alınarak modern kataliz teorilerinin temelini oluşturmuştur.
1.2. Modern Katalizin Rolü
Günümüzde, katalizörler şu temel alanlarda kritik öneme sahiptir:
- Enerji Üretimi: Petrol rafinasyonu ve yenilenebilir enerji teknolojileri.
- İlaç Sentezi: Yeni ilaçların üretiminde kullanılan hassas katalizörler.
- Çevre Koruma: Emisyon kontrol sistemlerinde kullanılan katalizörler, hava kirliliğini azaltır.
2. Katalizörlerin Bilimsel Temelleri
Kimyasal reaksiyonlar sırasında moleküllerin etkileşime girmesi ve bağların kırılıp yeniden oluşması gerekir. Bu süreçte, katalizörler reaksiyonun gerçekleşme hızını artırarak reaktanların daha az enerji harcamasını sağlar.
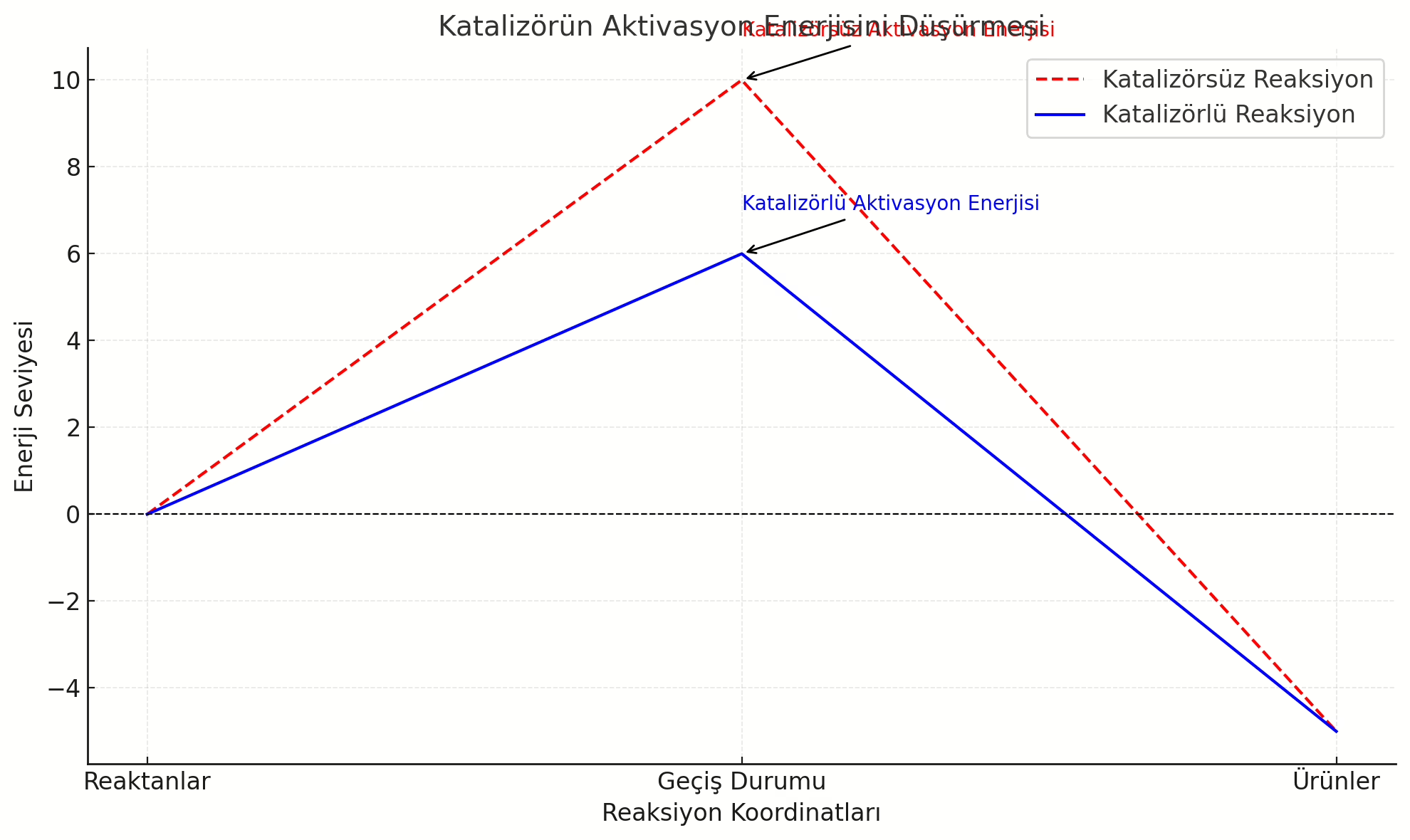
2.1. Aktivasyon Enerjisi ve Kataliz
Her kimyasal reaksiyonun başlaması için belirli bir enerjiye ihtiyaç vardır. Bu enerjiye aktivasyon enerjisi denir. Katalizörler, bu enerjiyi düşürerek reaksiyonun daha düşük enerji seviyelerinde gerçekleşmesini sağlar.
Örneğin:
- Katalizörsüz bir reaksiyonda aktivasyon enerjisi: 50 kJ/mol.
- Katalizörlü bir reaksiyonda aktivasyon enerjisi: 10 kJ/mol.
Bu enerji farkı, katalizörün sağladığı verimliliği açıkça gösterir.
2.2. Homojen ve Heterojen Kataliz
Katalizörler, reaksiyon ortamındaki faz durumuna göre sınıflandırılır:
- Homojen Kataliz: Reaktanlarla aynı fazda bulunur. Örnek: Esterleşme reaksiyonlarında sülfürik asit.
- Heterojen Kataliz: Reaktanlardan farklı bir fazda bulunur. Örnek: Platin katalizörler gaz fazındaki reaksiyonlarda.
2.3. Adsorpsiyon ve Reaksiyon Süreci
Heterojen katalizde, reaksiyon genellikle şu aşamalarda gerçekleşir:
- Adsorpsiyon: Reaktan molekülleri katalizör yüzeyine bağlanır.
- Aktivasyon: Moleküller katalizör yüzeyinde daha düşük enerjiyle aktive olur.
- Reaksiyon: Kimyasal bağlar kırılır ve yeniden oluşur.
- Desorpsiyon: Ürünler katalizör yüzeyinden ayrılarak reaksiyon ortamına geçer.
3. Katalizör Türleri
Katalizörler, farklı kimyasal reaksiyonlarda kullanılan birçok türde sınıflandırılabilir.
3.1. Geçiş Metali Katalizörleri
Geçiş metalleri, elektron dizilimleri ve reaktivite özellikleri sayesinde birçok reaksiyonda katalizör olarak kullanılır. Örnekler:
- Platin (Pt): Petrol rafinasyonunda kullanılır.
- Paladyum (Pd): Organik sentezde hidrojenasyon reaksiyonlarında etkilidir.
3.2. Enzimler (Doğal Katalizörler)
Enzimler, biyolojik süreçlerin hızlandırıcılarıdır. Örneğin:
- Amilaz: Nişastayı glikoza dönüştürür.
- DNA polimeraz: DNA replikasyonunu hızlandırır.
3.3. Asit ve Baz Katalizörleri
Kimyasal reaksiyonların hızını artırmak için asitler ve bazlar sıkça kullanılır:
- H₂SO₄ (Sülfürik Asit): Esterleşme reaksiyonlarında.
- NaOH (Sodyum Hidroksit): Sabun üretiminde.
3.4. Zeolitler
Zeolitler, gözenekli yapıları nedeniyle petrol moleküllerini ayrıştırma işlemlerinde kullanılır. Örnek:
- ZSM-5: Benzinin octan seviyesini artırır.
4. Endüstriyel Uygulamalar
4.1. Haber-Bosch Süreci
Amonyak üretiminde kullanılan bu yöntem, dünya çapında gübre üretiminin temelini oluşturur:
N2+3H2→2NH3N_2 + 3H_2 \rightarrow 2NH_3
Demir katalizör kullanılarak gerçekleşir.
4.2. Katalitik Konvertörler
Otomobil egzoz sistemlerinde kullanılan katalitik konvertörler, zararlı gazları daha az zararlı hale dönüştürür:
- CO → CO₂
- NOₓ → N₂
4.3. Polimer Sentezi
Ziegler-Natta katalizörleri, polietilen ve polipropilen gibi plastiklerin üretiminde kritik rol oynar.
5. Çevresel Etkiler
5.1. Pozitif Etkiler
- Emisyon Azaltma: Katalitik konvertörler, zararlı gazları çevreye salınımını azaltır.
- Enerji Tasarrufu: Daha düşük sıcaklık ve basınçlarda çalışılmasını sağlar.
5.2. Negatif Etkiler
- Katalizör üretimi sırasında kullanılan metallerin çıkarılması çevreye zarar verebilir.
- Kullanılmış katalizörlerin atık yönetimi, dikkatle ele alınmalıdır.
6. Geleceğin Katalizörleri
6.1. Nanoteknoloji Tabanlı Katalizörler
Nano boyutlu katalizörler, daha yüksek yüzey alanı ve reaktivite sunar. Örnek:
- Altın nanoparçacıkları: Oksidasyon reaksiyonlarında.
6.2. Yapay Zekâ ile Katalizör Tasarımı
Makine öğrenimi, yeni ve daha etkili katalizörlerin tasarımında devrim yaratmaktadır.
7. Sonuç
Katalizörler, kimyasal ve biyolojik süreçlerin temel taşıdır. Tarih boyunca oynadıkları rol, modern bilim ve teknolojinin gelişiminde kritik olmuştur. Gelecekte, daha verimli ve çevre dostu katalizörler, sürdürülebilir bir dünya için anahtar olacaktır.